(版本号:1.1;版本日期:2023年10月12日)
为了规范涉及人的生命科学和医学研究课题申报伦理审查管理,优化伦理委员会的审查流程,根据《涉及人的生命科学和医学研究伦理审查办法》《涉及人的生物医学研究伦理审查办法》等相关法规指南,制订课题申报伦理审查申请指南。所有我院承担的涉及人的生命科学和医学研究项目,均应在申报课题之前通过我院医学伦理委员会的伦理审查,获得伦理审查证明。
步骤一:准备伦理审查送审文件
按照以下伦理送审文件清单准备文件,在附件处获取“知情同意书模板和免除/免签知情同意书申请表”。知情同意书模板仅供参考,须根据研究项目实际情况撰写,知情同意书告知内容应完整全面,通俗易懂,知情同意书每一页的页眉处须注明版本号和版本日期。
1.项目申请书;
2.知情同意书或免除/免签知情同意书申请表。
步骤二:电脑端/手机端钉钉发起流程
电脑端/手机端钉钉选择工作台,下拉找到“科研管理”模块,点击“课题申报伦理审查”,进入“课题申报伦理审查”流程。
具体操作:
1.填写申报课题基本信息及文件上传。
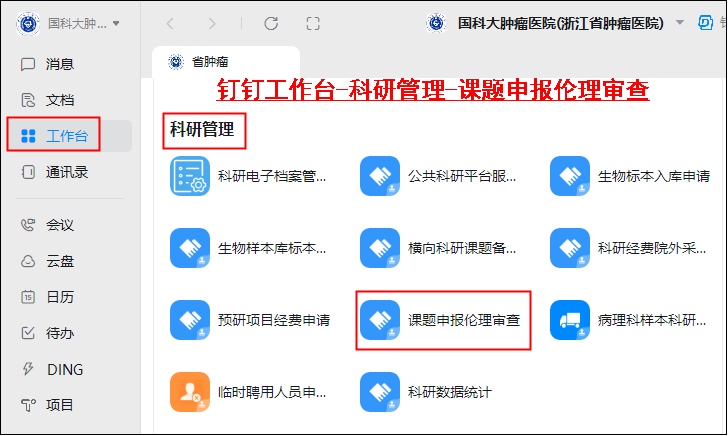
2.确认材料齐全后,点击“提交”。

注意事项:
1.课题申报前的伦理审查无需准备纸质资料给伦理办公室。
2.项目申报时项目申请书的题目和负责人姓名必须与伦理审查证明保持一致。请务必确定申报题目后再递交伦理审查,避免发生多次修改题目后导致伦理审查证明延误或题目与申报材料不一致等情况。
步骤三、伦理办公室形式审查
项目资料提交后,伦理秘书3个工作日内完成形式审查并反馈意见。
如项目通过形式审查,将进入下一流程阶段。
如被退回,可通过钉钉记录查看被退回原因,修改上传文件,重新提交新的流程。
步骤四、接受伦理审查
伦理委员会根据相关规定安排项目简易审查或会议审查。
如主审委员同意但提出修改意见,研究者须根据意见修改或回复,并将修改后的文件或回复内容通过钉钉单独发送给流程中负责审查的伦理秘书,秘书将修改后的文件或回复内容再次送委员审查。
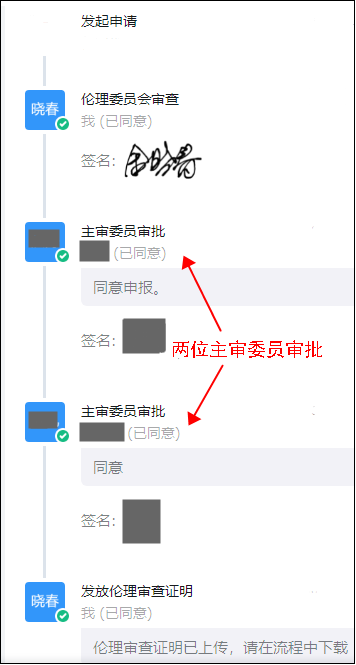
步骤五、下载伦理审查证明
审查结束后,伦理秘书上传伦理审查证明,请研究者在审批流程中下载。
如审查中有资料修改,伦理秘书会将修改后文件与证明一并上传。
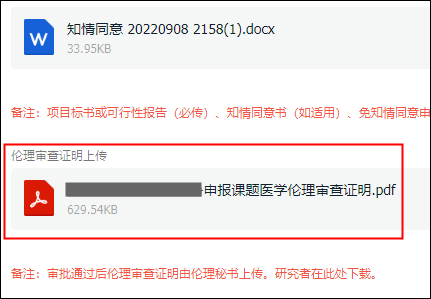
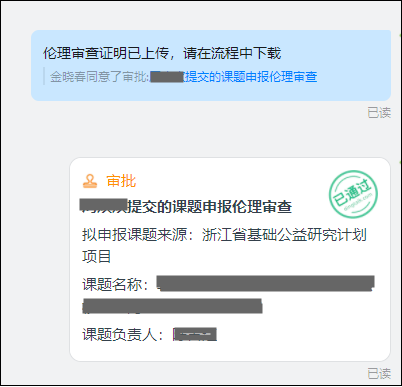
注意事项:
1.伦理审查证明通过钉钉审批流程上传提供电子版扫描件,不提供纸质版。
2.课题申报如获得立项,需重新按照科研项目伦理审查要求准备完整资料,在临床试验智能平台系统(CTMS)提交伦理审查申请,获得伦理审查批件后方能开展研究。
伦理办公室联系人:金晓春
联系电话:0571-88122564;地址:行政科研楼316室

Copyright © 2022 浙江省肿瘤医院 ALLRights Reserved 浙ICP备11008795号技术支持:新慧医联
